DNA 甲基化與癌癥
癌癥中 DNA 甲基化的改變已經(jīng)被認為是開發(fā)強大的診斷、預后和預測疾病發(fā)生生物標志物較有潛力目標。盡管有超過 14000 份文章中描述了基于 DNA 甲基化的生物標記物及其在癌癥中的臨床聯(lián)系,但只有 14 種生物標記物被轉化為商業(yè)化的臨床測試。方法上和實驗上的障礙都是造成這種巨大差異的主要原因,但是基于 DNA 甲基化的生物標記的基因組位置是一個內在的和必要的屬性,它也有一個重要的和經(jīng)常被忽視的作用。作者檢查了 DNA 甲基化的位置對癌癥生物標記物的發(fā)展的重要性,并通過商業(yè)上可獲得的測試,詳細研究了各種生物標記物的基因組位置和其他相關特征。作者還強調了公共數(shù)據(jù)庫對 DNA 甲基化發(fā)展的價值。
DNA 甲基化生物標志物
在 2003 年,Peter Laird 表達了他對 DNA 甲基化生物標志物的信心,他相信近期人們對 DNA 甲基化在人類癌癥中作用的理解所取得的進展,有一天會產生大量強有力的以 DNA 甲基化為基礎的生物標記物,特別是用于癌癥診斷。這種信念是基于大量的 DNA 甲基化的變化特征,使他們有成為生物標志物的前途:這些變化頻繁地發(fā)生在癌癥早期,容易被現(xiàn)有技術發(fā)現(xiàn),DNA 甲基化在固定的樣本中有穩(wěn)定性,各種體液和細胞類型特異性樣本中均存在。DNA 甲基化作為腫瘤標志物已經(jīng)被大量發(fā)表。為了更準確地定義這個數(shù)字,作者在 PubMed 數(shù)據(jù)庫中搜索描述 DNA 甲基化的生物標志物的出版物。根據(jù)對這些出版物中有代表性的子集進行人工整理,共檢索到 14,743 篇研究文章,估計有 1,800 個標志物。然而,只有 14 個以 DNA 甲基化為基礎的生物標記物目前已在市場上出售,共涉及 13 個基因:
1、Glutathione S- transferase P (GSTP1);
2、Adenomatous polyposis coli protein (APC);
3、Ras association domain- containingprotein 1 (RASSF1);
4、N- myc downregulated gene 4 (NDRG4);
5、Bone morphogenetic protein 3 (BMP3);
6、Septin-9 (SEPT9);
7、Short stature homeobox protein 2 (SHOX2);
8、Twist related protein 1 (TWIST1);
9、Homeobox protein OTX1 (OTX1);
10、One cut domain family member 2 (ONECUT2);
11、Methylated-DNA-protein- cysteine methyltransferase (MGMT);
12、Branched- chain-amino- acid aminotransferase, cytosolic (BCAT1);
13、DNA- binding protein Ikaros (IKZF1)。
這 14 種生物標志物,只有 9 種(GSTP1,APC、RASSF1、NDRG4、BMP3、兩個 SEPT9 生物標志物、SHOX2 和 MGMT) 已被納入一個或多個臨床指南。此外,只有兩項測試獲得了 FDA 的批準:結腸衛(wèi)士(NDRG4 和 BMP3) 用于分析糞便樣本 DNA 和 Epi proColon (SEPT9) 用于便潛血的檢測。甲基化標志物轉化的成功率也就 0.8%。
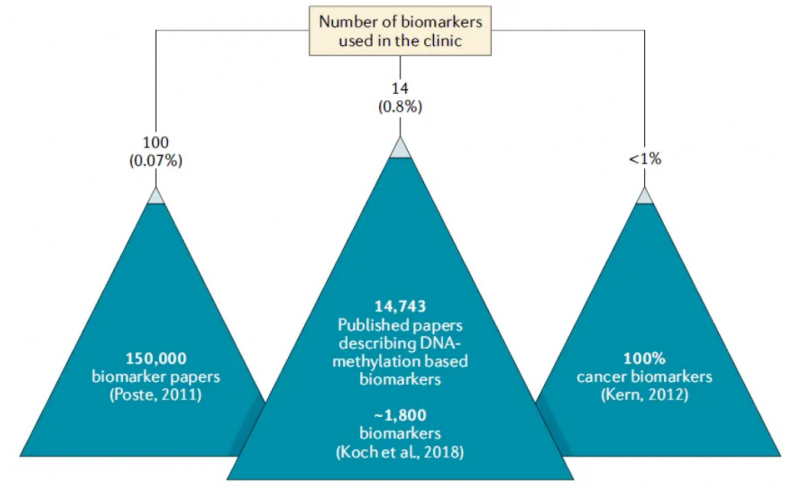
DNA 甲基化標志物的臨床轉化
上述的轉化成功率以及目前公眾對科學研究的可靠性和效率的討論,都值得作者反思,為什么很少有 DNA 甲基化的生物標記從發(fā)現(xiàn)和發(fā)表過渡到臨床試驗。這個問題的答案是復雜的、多方面的,主要與小樣本測試和缺乏實質性的臨床價值,以及各種方法的說明(如有偏差的病人選擇、研究設計和數(shù)據(jù)分析不當,缺乏驗證和 / 或不恰當?shù)膱蟾妫@些妨礙了徹底評估生物標志物的臨床價值。此外,開發(fā)定量分析特定生物標志物(包括提供驗證和探索臨床應用的試驗)所需的資金投入是一個主要障礙。這些問題并不是基于 DNA 甲基化的生物標志物所特有的。生物標志物研究領域的研究人員普遍面臨著類似的問題,盡管這些問題直到現(xiàn)在才開始得到解決。
除了圍繞臨床轉化已有的問題,作者相信在癌癥患者 DNA 甲基化生物標志物的發(fā)現(xiàn)和臨床應用之間存在另一個經(jīng)常被忽視的障礙。在 2011 年的時候,作者就發(fā)文強調過甲基化所在基因組位置對于生物標志物應用的重要性。作者認為,更好地理解和更詳細地分析 DNA 甲基化的基因組位置的臨床相關性,可以增加成功被轉化的生物標志物的數(shù)量。從這個角度來看,目前公開的表觀基因組數(shù)據(jù)為更好地選擇基于 DNA 甲基化的生物標志物的位置提供了機會。
位置的重要性
傳統(tǒng)上,DNA 甲基化研究和基于 DNA 甲基化的生物標志物研究主要集中于腫瘤抑制基因啟動子 CpG 島的高甲基化效應。然而,即使在單個啟動子區(qū)域內,并非所有 CpG 島在功能上都是相同的。例如,轉錄沉默通常是由啟動子的一個或多個小部分的甲基化控制的,而不是由整個啟動子區(qū)域控制的。因此,識別臨床相關 CpG 島的準確定位是發(fā)展 DNA 甲基化的生物標志物研究的重要一步。
應用于診斷的甲基化標志物
在一些研究中,GSTP1 的甲基化已被報道為一種很有前途的肝細胞癌(HCC) 診斷標志物,但特異性水平差異很大。這種差異被假設為是由于檢測同一啟動子的不同特定部分的造成的。研究人員采用亞硫酸氫鹽測序發(fā)現(xiàn),GSTP1 啟動子的 5?區(qū)域區(qū)分肝細胞癌和非惡性肝細胞癌肝臟疾病或沒有確定的病理改變的肝臟組織特異性更強比 3?啟動子(分別為 97.1% 和 60%; P <0.001)。同一研究團隊,在研究 RASSF1 的甲基化作為 HCC 早篩標志物時得出類似的結論(特異性依次為 72.9%,27.1% 和 38.6%,敏感性為固定的 90%;p<0.0001)。
預后甲基化標記
在之前的研究中,作者分析了 GREM1 啟動子 CpG 島內的三個不同的基因組區(qū)域,發(fā)現(xiàn)在這些區(qū)域中,只有一個區(qū)域的 CpGs 甲基化與透明細胞腎細胞癌(RCC) 患者的不良預后相關;風險比(HR) 2.32, 95% CI 1.52-3.53;P = 0.001)。胃癌患者也觀察到類似的結果,MAL 啟動子區(qū)的甲基化與胃癌的預后相關,并下調基因表達,該特定的啟動子區(qū)域高甲基化靠近轉錄起始位點(TSS)。研究人員描述了位于 CpG 島外的 NMDAR2B 基因啟動子的一個小區(qū)域的甲基化與食管鱗狀細胞癌患者和疾病特異性生存結果之間的關系(HR 3.13, 95%) 可信區(qū)間 1.05 - -9.72;P≤0.006),而 DNA 甲基化在另外兩個位置,位于 TSS 下游和內側 CpG 島與患者預后無相關性。
有趣的是,單個 CpG 二核苷酸的甲基化狀態(tài),而不是包含多個 CpG 二核苷酸更廣泛區(qū)域的甲基化狀態(tài)已經(jīng)被證明會影響基因表達的調控。在 CLL 中,ZAP70 基因經(jīng)過高分辨率的甲基化掃描后發(fā)現(xiàn),一個單 CpG 位點(TSS 下游 233bp 處)的甲基化狀態(tài)與病人的預后顯著相關。
早篩的甲基化標志物
在描述 MGMT 甲基化對膠質母細胞瘤患者的預測力的研究中,MGMT 的甲基化狀態(tài)是通過甲基化特異性來評估的 PCR (MSP),使用引物僅覆蓋 MGMT 基因的外顯子和啟動子區(qū)域的少量 CpG 二核苷酸。甲基化與 MGMT 表達和 / 或活性之間的直接相關性未被研究。在這一發(fā)現(xiàn)之后,許多 25 - 27 歲的研究者使用諸如焦磷酸測序等定量技術對 MGMT 基因的啟動子區(qū)域進行了更詳細的分析。這些研究的目的是為了對特定的甲基化模式有更深入的了解,以確定 轉錄調控中是重要的 CpG 二核苷酸,并確定臨床價值的甲基化變化區(qū)域。已經(jīng)發(fā)表的關于與 MGMT 表達相關的特定甲基化區(qū)域,甚至單個 CpG 二核苷酸的結果是相互矛盾的。商業(yè)化的 PredictMDx 產品測試所覆蓋含的 CpGs 75-78 區(qū)域是目前研究建議的區(qū)域,該區(qū)域的 CpG 二核苷酸甲基化已被反復證明與有利的患者預后相關。
基因組結構
特定 CpG 二核苷酸在單個基因組區(qū)域的甲基化,可以調節(jié)轉錄,也可以決定生物標志物的臨床價值。因此,確定一個潛在的相關的基因組位置對以 DNA 甲基化為基礎的生物標志物很重要。除了位置之外,DNA 甲基化的基因組背景也必須考慮,例如,不同功能區(qū)域的存在,如外顯子或增強子。這些不同區(qū)域的存在與甲基化特征有關。啟動子區(qū) CpG 島往往是低甲基化的,而基因 body 區(qū),特別是外顯子區(qū)往往是甲基化的。2012 年發(fā)表的研究表明,在發(fā)育和疾病過程中,基因間區(qū)和基因內區(qū) DNA 甲基化的改變都受到調節(jié),這些改變積極參與了轉錄的調控。非啟動子位點的甲基化在幾個重要過程的調控中發(fā)揮作用,包括剪接、來自替代啟動子的替代轉錄本的表達和增強子激活,盡管這種 DNA 修飾仍然是生物標志物開發(fā)的一個很大程度上未被探索的領域。然而,潛在的臨床應用已經(jīng)證明甲基化為基礎的生物標志物在某些非啟動子位置。例如,對于 15q25 染色體區(qū)域的多個鄰近基因的長期表觀遺傳沉默(LRES) 呈陽性的胃癌患者,其疾病復發(fā)的風險較低(HR 0.6;95% 可信區(qū)間 0.38 - -0.94;P = 0.027)。異常增強子高甲基化也被證明是預后的患者生存 RCC (log- rank P < 0.05)。隨著作者對這些類型的 DNA 甲基化模式的生物學和效應的理解進步,作者將毫無疑問地看到,啟動子區(qū)域之外的甲基化生物標志物數(shù)量將會增加。
生物標志物的發(fā)展
為了使特定基因組位置的甲基化成為一個良好的生物標志物,必須在臨床檢測出感興趣的組之間甲基化的顯著差異:
例如,作為診斷生物標志物區(qū)分腫瘤和非腫瘤組織; 預后標記區(qū)分高危疾病患者和低危疾病患者; 或者預測標記區(qū)分有反應者和無反應者之間。理想情況下,相關基因在兩組之間應該有差異表達。候選診斷生物標志物的一個經(jīng)典例子是腫瘤抑制基因啟動子的高甲基化。甲基化和基因表達之間的聯(lián)系提供了一個清晰的生物學原理,但基于 DNA 甲基化的生物標記不一定與基因表達的可測量變化相關聯(lián)。例如,在商業(yè)化的生物標志物中,有 4 個(APC、RASSF1 和 SEPT9 兩個生物標志物)沒有顯示 DNA 甲基化和相關基因表達之間的相關性。
結論
十多年前,以 DNA 甲基化為基礎的生物標記物被認為是癌癥生物標記物研究的下一個“大事件”,但到目前為止,它們一直難以達到預期。對于為什么如此之少以 DNA 甲基化為基礎的生物標記物商業(yè)化,有幾種可能的解釋,但作者認為 DNA 甲基化與其高精度的基因組位置之間的復雜關系是主要障礙之一。為了減少已發(fā)表的生物標志物數(shù)量和臨床使用的生物標志物數(shù)量之間的差異,作者制定了三個簡單的建議來開發(fā)基于 DNA 甲基化的生物標志物。根據(jù)這些建議開發(fā)的生物標志物并不能保證是可重復的或臨床相關的,但是,至少 DNA 甲基化的生物標志物障礙,確定臨床相關的區(qū)域,可以通過分析公開可用的數(shù)據(jù)來克服。為了系統(tǒng)地評估基于 DNA 甲基化的生物標記物的表現(xiàn),并支持未來對此類生物標記物的發(fā)現(xiàn)和驗證的準確報告,作者正在開發(fā)一個包含所有已發(fā)表生物標記物數(shù)據(jù)庫,以及一個生物標記物的報告標準。作者希望這些建議和持續(xù)的努力將有助于提高基于 DNA 甲基化的標記的性能,促進可重復性,并減少目前在這一領域產生的研究浪費。
更多伯豪生物服務


